Metale ciężkie to pierwiastki chemiczne o gęstości powyżej 5 g/cm³ i dużej masie atomowej. Ze względu na swoje specyficzne właściwości fizyczne i chemiczne są one wykorzystywane w wielu procesach przemysłowych. Do najczęściej występujących metali ciężkich w ściekach przemysłowych należą ołów (Pb), miedź (Cu), cynk (Zn), nikiel (Ni), chrom (Cr), kadm (Cd) i rtęć (Hg). Metale te są jednak toksyczne nawet w niskich stężeniach i dlatego stanowią poważne wyzwanie dla oczyszczania wody i ścieków.
Spis treści
Przemysłowe źródła metali ciężkich
Przemysłowe wykorzystanie metali ciężkich prowadzi do ich przedostawania się do ścieków. Zanieczyszczenie to zależy w dużej mierze od odpowiednich procesów i przemysłu. Metale ciężkie mogą przedostawać się do środowiska poprzez ścieki, wodę płuczącą lub pozostałości produkcyjne. Poniżej opisano najważniejsze źródła przemysłowe:
Galwanizacja i obróbka powierzchni
- Zastosowanie:
- Nikiel, chrom i cynk są stosowane w galwanotechnice do powlekania metali w celu uzyskania ochrony przed korozją, twardości lub właściwości dekoracyjnych.
- Metale ciężkie w ściekach:
- Typowe zanieczyszczenia to chrom(VI), nikiel, cynk i miedź.
- Wyzwania:
- Woda do płukania często zawiera kombinację różnych metali ciężkich, co utrudnia ukierunkowaną separację.
Obróbka metalu
- Produkcja stali i aluminium:
- Pozostałości po wytopie i przetwarzaniu metali zawierają metale ciężkie, takie jak kadm, cynk i ołów.
- Produkcja narzędzi i inżynieria mechaniczna:
- Ścieki często zawierają zanieczyszczenia miedzią i niklem pochodzące ze smarów i chłodziw, a także z technologii produkcji.
- Przemysł motoryzacyjny:
- Metale ciężkie, takie jak cynk, chrom i miedź, są uwalniane do ścieków podczas produkcji pojazdów, w szczególności podczas malowania, powlekania i produkcji komponentów.
Górnictwo i przetwarzanie rudy
- Zastosowanie:
- Wydobycie metali takich jak miedź, cynk czy ołów oraz przetwarzanie rud powoduje powstawanie ścieków o wysokim stężeniu żelaza, manganu, kadmu i innych metali.
- Wyzwania:
- Ścieki z kopalń są często kwaśne (tzw. "kwaśny drenaż kopalniany") i zawierają metale ciężkie w postaci rozpuszczonej.
Przemysł chemiczny i petrochemiczny
- Zastosowanie:
- Metale ciężkie, takie jak rtęć, nikiel i chrom, są wykorzystywane jako katalizatory w reakcjach chemicznych.
- Metale ciężkie w ściekach:
- Pozostałości z procesów katalitycznych i zanieczyszczenia w surowcach przyczyniają się do zanieczyszczenia metalami ciężkimi.
Przemysł elektroniczny i elektryczny
- Zastosowanie:
- Metale ciężkie, takie jak miedź, ołów i cyna, są niezbędne do produkcji płytek drukowanych, baterii i komponentów elektronicznych.
- Metale ciężkie w ściekach:
- Materiały lutownicze, procesy galwaniczne i czyszczenie komponentów prowadzą do narażenia na ołów, cynk, nikiel i miedź.
Przemysł farb, lakierów i pigmentów
- Zastosowanie:
- Metale ciężkie, takie jak chrom, ołów i kadm, są stosowane jako pigmenty barwiące i środki stabilizujące.
- Metale ciężkie w ściekach:
- Ścieki często zawierają pozostałości z produkcji, które są toksyczne i trudne do biodegradacji.
Przemysł szklarski i ceramiczny
- Zastosowanie:
- Metale ciężkie, takie jak ołów i kadm, są wykorzystywane w produkcji szkła i szkliw ceramicznych.
- Wyzwania:
- Ścieki często zawierają związki metali, które są trudne do rozpuszczenia i wymagają specjalnego oczyszczania.
Wpływ metali ciężkich na środowisko i zdrowie
Toksyczność i bioakumulacja
Metale ciężkie nie ulegają biodegradacji i gromadzą się w środowisku. Nawet niewielkie ich ilości mogą powodować znaczne szkody w ekosystemach:
- Chrom(VI): Wysoce toksyczny i rakotwórczy; często stosowany w procesach galwanicznych.
- Nikiel: Drażniący i alergizujący; powszechne zanieczyszczenie w ściekach przemysłowych.
- Rtęć: Neurotoksyczna i niezwykle trwała; ulega bioakumulacji w organizmach wodnych.
- Kadm: Powoduje uszkodzenie nerek i kości; często spotykany w bateriach i pigmentach.
Wpływ na systemy techniczne
- Korozja:
- Metale ciężkie w wodzie sprzyjają korozji elektrochemicznej rur i systemów.
- Zakłócenie procesów biologicznych:
- Metale ciężkie hamują mikroorganizmy, które rozkładają substancje organiczne w biologicznych oczyszczalniach ścieków, a tym samym zakłócają wydajność oczyszczania.
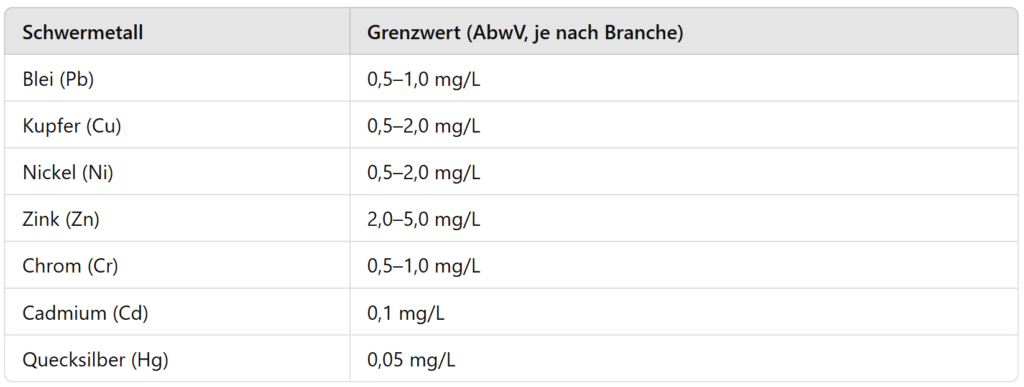
Dopuszczalne wartości dla metali ciężkich w ściekach przemysłowych
Zrzut metali ciężkich do zbiorników wodnych lub publicznych systemów kanalizacyjnych jest ściśle regulowany. Niemieckie rozporządzenie w sprawie ścieków (AbwV) określa limity branżowe, których należy przestrzegać w celu zminimalizowania zanieczyszczenia środowiska.
Proces usuwania metali ciężkich z wody i ścieków
Wybór technologii oczyszczania zależy od stężenia, rodzaju metalu ciężkiego i wymagań dotyczących jakości wody. Systemy CP są często łączone z wymiennikami j onowymi lub filtrami z węglem aktywnym.
1. wytrącanie i flokulacja w zakładach CP
Strącanie chemiczne jest kluczowym procesem w oczyszczaniu wody i ścieków w celu usunięcia metali ciężkich. Proces ten opiera się na chemicznej konwersji rozpuszczonych jonów metali ciężkich w słabo rozpuszczalne związki, które następnie można usunąć z wody poprzez sedymentację, flotację lub filtrację.
Mechanizm wytrącania
Reakcja z jonami wodorotlenkowymi (wytrącanie wodorotlenków):
- Dodanie zasad, takich jak mleko wapienne (Ca(OH)₂) lub soda kaustyczna (NaOH), prowadzi do wzrostu wartości pH, powodując wytrącanie się jonów metali ciężkich w postaci trudno rozpuszczalnych wodorotlenków metali.
- W ten sposób powstają osady wodorotlenku metalu, które można oddzielić od wody ze względu na ich niską rozpuszczalność.
Reakcja z siarczkami (wytrącanie siarczków):
- W przypadku metali ciężkich o szczególnie niskiej rozpuszczalności w postaci siarczku (np. rtęć, ołów) stosuje się jony siarczkowe, zazwyczaj z siarczku sodu (Na₂S).
- Siarczki mają tę zaletę, że tworzą stabilne osady nawet przy lekko kwaśnych wartościach pH.
Wytrącanie za pomocą czynników kompleksujących:
- W przypadkach, gdy metale ciężkie są obecne w stabilnych kompleksach (np. z powodu czynników chelatujących, takich jak EDTA), mogą być wymagane specjalne odczynniki do rozbicia kompleksów przed wytrąceniem.
Czynniki wpływające na opady
Skuteczność wytrącania zależy od różnych czynników chemicznych i fizycznych, które muszą być dokładnie kontrolowane:
Wartość pH:
- Wartość pH jest najważniejszym parametrem, ponieważ rozpuszczalność większości wodorotlenków metali ciężkich jest silnie zależna od wartości pH.
- Przykłady:
- Wodorotlenek cynku wytrąca się optymalnie przy pH 9-10.
- Wodorotlenek żelaza(III) wytrąca się przy wartości pH 6-8.
- Precyzyjna kontrola wartości pH jest konieczna, ponieważ inne metale (np. aluminium) mogą stać się ponownie rozpuszczalne, jeśli wartość pH jest zbyt wysoka.
Stężenie odczynników:
- Do związania wszystkich jonów metali ciężkich wymagana jest wystarczająca ilość środka strącającego. Przedawkowanie może jednak prowadzić do zwiększenia kosztów operacyjnych i dodatkowego zużycia środków chemicznych.
Temperatura:
- Szybkość reakcji i rozpuszczalność produktów strącania zależą od temperatury. Wyższe temperatury generalnie sprzyjają szybkości reakcji.
Intensywność mieszania i czas kontaktu:
- Dobre mieszanie zapewnia intensywny kontakt odczynników z jonami metali ciężkich.
- Czas kontaktu musi być wystarczająco długi, aby reakcje chemiczne zaszły całkowicie.
Zakłócenia powodowane przez inne jony:
- Aniony, takie jak chlorek lub siarczan, mogą zwiększać rozpuszczalność niektórych związków metali ciężkich, a tym samym zmniejszać skuteczność wytrącania.
- W takich przypadkach wymagane są dodatkowe odczynniki strącające lub etapy obróbki wstępnej.
Flokulacja: stabilizacja i separacja produktów strącania
Po wytrąceniu powstałe produkty wytrącania często pozostają rozproszone w wodzie w postaci drobnych cząstek. Flokulacja służy do łączenia tych cząstek w większe agregaty (kłaczki), które są łatwiejsze do osadzenia lub oddzielenia.
Mechanizm flokulacji
- Koagulacja:
- Poprzez dodanie koagulantów, takich jak sole żelaza(III) lub glinu, elektrostatyczne siły odpychające między cząstkami są zmniejszone, co ułatwia ich aglomerację.
- Flokulacja:
- Flokulanty, takie jak polimery (np. poliakrylamidy), zwiększają tworzenie się cząstek poprzez wiązanie kłaczków ze sobą za pomocą mostków.
Granice wytrącania i flokulacji
Skompleksowane metale ciężkie:
- Metale ciężkie obecne w stabilnych kompleksach organicznych lub nieorganicznych są trudne do wytrącenia. Konieczne jest wcześniejsze rozszczepienie kompleksów (np. przez utlenianie lub redukcję).
Stężenia resztkowe:
- Die chemische Fällung erreicht häufig nicht die extrem niedrigen Restkonzentrationen (< 0,01 mg/l) , die in manchen Industrien erforderlich sind. In solchen Fällen sind ergänzende Verfahren wie Adsorption oder Ionenaustausch erforderlich.
Produkcja osadu:
- Wytrącanie generuje duże ilości szlamu opadowego, który musi zostać przetworzony i usunięty jako odpad niebezpieczny. Koszty utylizacji mogą być znaczne.
Chrom(VI):
- Metale ciężkie, takie jak chrom(VI), muszą zostać zredukowane do mniej toksycznej formy chromu(III) przed wytrąceniem, na przykład poprzez dodanie wodorosiarczynu sodu.

Zdjęcie: Nasz system CP ALMA CHEM MCW z wytrącaniem i flokulacją, odwadnianiem osadu oraz filtrem wielowarstwowym i wymiennikiem jonowym (w razie potrzeby).
2. wymiana jonowa
Wymiana jonowa to proces fizykochemiczny, w którym rozpuszczone w wodzie jony są zastępowane jonami w stałej żywicy jonowymiennej. Proces ten opiera się na specyficznym wiązaniu kationów lub anionów z aktywnymi grupami w materiale żywicy. Ze względu na wysoką selektywność żywic, metale ciężkie mogą być usuwane nawet z bardzo rozcieńczonych roztworów.
Mechanizm wymiany jonowej
- Wymiana kationów:
- Kationy metali ciężkich, takie jak Cu²⁺, Zn²⁺ lub Pb²⁺ są zastępowane jonami H⁺ (żywice na bazie wodoru) lub Na⁺ (żywice na bazie sodu).
- Jony metali ciężkich są wiązane z matrycą żywicy i usuwane z wody.
- Wymiana anionowa:
- Ujemnie naładowane kompleksy metali ciężkich, takie jak chromiany (CrO₄²-), są zastępowane przez jony OH-.
Rodzaje wymieniaczy jonowych
Silne wymieniacze kationowe:
- Skutecznie usuwa metale ciężkie, takie jak miedź, nikiel i cynk z roztworów kwaśnych.
- Może być stosowany przy wartościach pH od 1 do 14.
Słabe wymieniacze kationowe:
- Skuteczny przy średnich i wysokich wartościach pH; idealny do roztworów lekko kwaśnych do obojętnych.
Silne wymieniacze anionowe:
- Usunąć ujemnie naładowane kompleksy, takie jak chromiany lub arseniany.
- Stosować w roztworach alkalicznych.
Żywice selektywne:
- Opracowany dla określonych metali ciężkich, takich jak rtęć, kadm lub chrom.
Czynniki wpływające na wymianę jonową
stężenie jonów:
- Wymiana jonowa jest szczególnie skuteczna przy niskich stężeniach, ponieważ żywice mają wysokie powinowactwo do jonów metali ciężkich.
Wartość pH:
- Der pH-Wert beeinflusst die Ladung der Schwermetalle und somit ihre Bindung an das Harz. Beispielsweise liegt Eisen bei pH < 3 als Fe³⁺ vor und kann leicht entfernt werden, während es bei höheren pH-Werten zu Hydroxid fällt.
Konkurs:
- Obecność innych kationów, takich jak Ca²⁺ lub Mg²⁺ może zmniejszyć skuteczność wymiany jonowej.
Pojemność żywicy:
- Maksymalne obciążenie żywicy jest ograniczone przez jej pojemność właściwą (równoważnik jonów na objętość).
Regeneracja:
- Po osiągnięciu limitu wydajności żywica jest regenerowana przy użyciu środków chemicznych, takich jak kwas solny (HCl) lub soda kaustyczna (NaOH).
Zalety i ograniczenia wymiany jonowej
Zalety:
- Bardzo wysoka selektywność, nawet w przypadku niskich stężeń metali ciężkich.
- Możliwość regeneracji, co obniża koszty eksploatacji.
- Możliwość dostosowania do określonych metali (np. chromu lub miedzi).
Limity:
- Ograniczona wydajność przy wysokich stężeniach.
- Konkurencja ze strony innych jonów może zmniejszyć wydajność.
- Chemikalia regeneracyjne generują dodatkowe ścieki.

Zdjęcie: Nasz system wymiennika jonów ALMA ION z filtrem z węglem aktywnym ALMA FIL AK.
3. adsorpcja na węglu aktywnym
Adsorpcja przy użyciu filtrów z węglem aktyw nym opiera się na fizycznej lub chemicznej adsorpcji jonów metali ciężkich lub kompleksów metali ciężkich na powierzchni porowatego materiału, takiego jak węgiel aktywny. Duża wewnętrzna powierzchnia węgla aktywnego służy do wiązania rozpuszczonych substancji z wody.
Mechanizm adsorpcji
- Adsorpcja fizyczna:
- Metale ciężkie są utrzymywane na powierzchni węgla aktywnego przez siły van der Waalsa lub oddziaływania elektrostatyczne.
- Chemisorpcja:
- Metale ciężkie tworzą wiązania chemiczne z grupami funkcyjnymi na powierzchni węgla aktywnego (np. grupami karboksylowymi lub hydroksylowymi).
Rodzaje węgla aktywnego
Sproszkowany węgiel aktywny (PAH):
- Drobny proszek dodawany bezpośrednio do wody.
- Szczególnie nadaje się do obróbki wsadowej.
Granulowany węgiel aktywny (GAK):
- Gruboziarnisty węgiel aktywny stosowany w filtrach.
- Możliwe długotrwałe i ciągłe użytkowanie.
Impregnowany węgiel aktywny:
- Poddane działaniu odczynników chemicznych (np. siarki) w celu skutecznego usunięcia określonych metali ciężkich, takich jak rtęć lub arsen.
Czynniki wpływające na adsorpcję
stężenie metali ciężkich:
- Wyższe stężenia prowadzą do lepszego wykorzystania pojemności adsorpcyjnej, ale także do szybszego nasycenia.
Wartość pH:
- Wartość pH wpływa na ładunek jonów metali ciężkich i ładunek powierzchniowy węgla aktywnego.
- Przykład:
- Przy niskiej wartości pH metale ciężkie, takie jak Pb²⁺, są naładowane dodatnio i dobrze wiążą się z ujemnie naładowanym węglem aktywnym.
Temperatura:
- Procesy adsorpcji są zwykle egzotermiczne, więc zwiększenie temperatury może zmniejszyć wydajność.
Struktura porów:
- Rozmiar i rozkład porów w węglu aktywnym wpływa na zdolność wiązania.
Optymalizacja adsorpcji
- Wstępne uzdatnianie wody:
- Usuwanie zawieszonych ciał stałych i związków organicznych poprawia skuteczność.
- Zastosowanie impregnowanego węgla aktywnego:
- Specjalnie przetworzony węgiel aktywny jest znacznie bardziej skuteczny w przypadku metali ciężkich, takich jak arsen i rtęć.
- Regeneracja:
- Nasycenie węgla aktywnego można odwrócić za pomocą procesów termicznych lub chemicznych, co zmniejsza koszty operacyjne.
Zalety i ograniczenia adsorpcji na węglu aktywnym
Zalety:
- Wysoka wydajność przy niskim stężeniu metali ciężkich.
- Wszechstronny w użyciu, również do innych zanieczyszczeń, takich jak związki organiczne.
- Może być impregnowany pod kątem określonych metali ciężkich.
Limity:
- Ograniczona pojemność materiałów adsorpcyjnych.
- Regeneracja jest energochłonna i chemiczna.
- Mniej odpowiednie dla wysokich stężeń metali ciężkich.

Zdjęcie: Nasze filtry z węglem aktywnym ALMA FIL AK z filtrem wielowarstwowym ALMA FIL.
Wnioski
Oczyszczanie ścieków zanieczyszczonych metalami ciężkimi pochodzącymi z procesów przemysłowych jest jednym z głównych wyzwań związanych z uzdatnianiem wody. Specyficzne wymagania dotyczące oczyszczania ścieków różnią się znacznie w zależności od branży i procesu produkcyjnego. Dzięki zaawansowanym technologiom, takim jak strącanie i flokulacja w instalacjach CP, wymiana jonowa i adsorpcja na węglu aktywnym, można niezawodnie spełnić limity prawne i zminimalizować wpływ na środowisko.
Aby uzyskać więcej informacji na temat naszych produktów, prosimy skontaktować się z nami w dowolnym momencie!








