Redukcia ťažkých kovov označuje proces odstraňovania alebo minimalizácie ťažkých kovov vo vodných a odpadových systémoch. Ťažké kovy ako meď (Cu), nikel (Ni), chróm (Cr), zinok (Zn), kadmium (Cd) a olovo (Pb) predstavujú vzhľadom na svoju toxicitu a perzistenciu v životnom prostredí jednu z najväčších výziev v oblasti úpravy vody a odpadových vôd. Ich efektívna redukcia je rozhodujúca pre dodržiavanie zákonných limitov, ochranu životného prostredia a zabezpečenie kvality vody pre priemyselné procesy.
Obsah
Technické pozadie a charakteristiky ťažkých kovov
Chemické vlastnosti ťažkých kovov
- rozpustnosť:
- Ťažké kovy môžu byť prítomné vo forme rozpustených iónov, komplexov alebo častíc. Ich rozpustnosť závisí vo veľkej miere od hodnoty pH a chemického prostredia.
- Príklad: Chróm(VI) je vysoko rozpustný v neutrálnej až alkalickej vode, zatiaľ čo chróm(III) sa vysráža vo forme hydroxidu.
- oxidačné stavy:
- Niektoré ťažké kovy, ako je chróm alebo železo, sa vyskytujú v rôznych stupňoch oxidácie, čo ovplyvňuje výber redukčného procesu.
- tvorba komplexov:
- Ťažké kovy môžu vytvárať stabilné komplexy s organickými látkami (napr. EDTA), čo sťažuje ich odstraňovanie.
Výzvy v oblasti redukcie ťažkých kovov
- Vysoká toxicita:
- Ťažké kovy majú toxický vplyv na vodné ekosystémy a sú škodlivé pre ľudské zdravie.
- Regulačné požiadavky:
- Dodržiavanie zákonných limitných hodnôt je často možné len pomocou zložitých a viacfázových postupov.
- Rozmanitosť zloženia odpadových vôd:
- Priemyselné odpadové vody môžu obsahovať vysoké koncentrácie ťažkých kovov, organických látok a iných rušivých látok, ktoré si vyžadujú špecifické prístupy k spracovaniu.
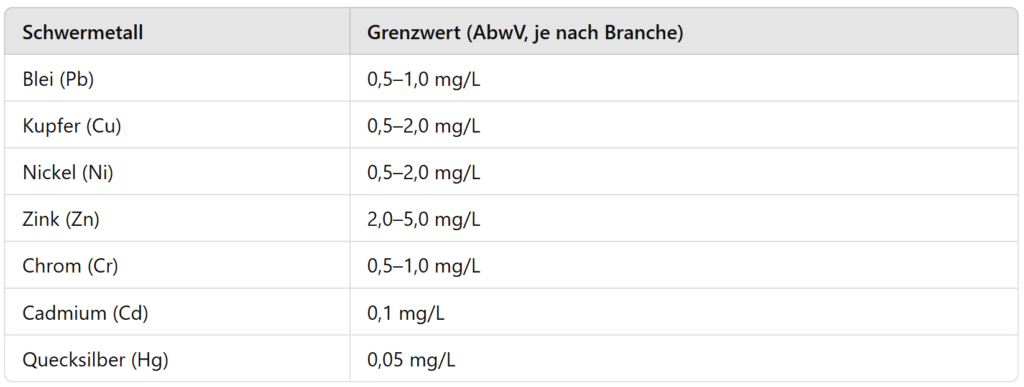
Hraničné hodnoty pre ťažké kovy v priemyselných odpadových vodách
Vypúšťanie ťažkých kovov do vôd alebo verejných kanalizačných systémov je prísne regulované. Nariadenie o odpadových vodách (AbwV) stanovuje odvetvové limitné hodnoty, ktoré je potrebné dodržiavať, aby sa minimalizovalo zaťaženie životného prostredia.
Postup na odstraňovanie ťažkých kovov z vody a odpadových vôd
Výber technológie úpravy závisí od koncentrácie, druhu ťažkého kovu a požiadaviek na kvalitu vody. Často sa zariadenia CP kombinujú s iónovými výmenníkmi alebo filtrami s aktívnym uhlím.
1. Zrážanie a flokulácia v zariadeniach CP
Chemická precipitácia je kľúčovým procesom pri úprave vody a čistení odpadových vôd na odstraňovanie ťažkých kovov. Proces je založený na chemickej premene rozpustených iónov ťažkých kovov na ťažko rozpustné zlúčeniny, ktoré sa následne môžu odstrániť z vody sedimentáciou, flotáciou alebo filtráciou.
Mechanizmus zrážania
Reakcia s hydroxidovými iónmi (hydroxidová precipitácia):
- Prídavok zásad, ako je vápenné mlieko (Ca(OH)₂) alebo hydroxid sodný (NaOH), vedie k zvýšeniu hodnoty pH, čím sa ťažké kovové ióny vysrážajú vo forme ťažko rozpustných kovových hydroxidov.
- Pri tom vznikajú zrazeniny hydroxidov kovov, ktoré sa vďaka svojej nízkej rozpustnosti dajú od vody odseparovať.
Reakcia so sulfidmi (sulfidová precipitácia):
- Pre ťažké kovy s obzvlášť nízkou rozpustnosťou ako sulfid (napr. ortuť, olovo) sa používajú sulfidové ióny, typicky zo sulfidu sodného (Na₂S).
- Sulfidy majú tú výhodu, že vytvárajú stabilné zrazeniny aj pri mierne kyslých hodnotách pH.
Zrážanie komplexotvornými činidlami:
- V prípadoch, keď sú ťažké kovy prítomné v stabilných komplexoch (napr. prostredníctvom chelatačných činidiel, ako je EDTA), môžu byť pred zrážaním potrebné špeciálne činidlá na rozloženie komplexov.
Faktory ovplyvňujúce zrážanie
Účinnosť zrážania závisí od rôznych chemických a fyzikálnych faktorov, ktoré je potrebné starostlivo kontrolovať:
Hodnota pH:
- Hodnota pH je najdôležitejší parameter, pretože rozpustnosť väčšiny hydroxidov ťažkých kovov vo veľkej miere závisí od hodnoty pH.
- Príklady:
- Hydroxid zinočnatý sa optimálne vysráža pri pH 9–10.
- Hydroxid železitý sa vyskytuje už pri hodnote pH 6–8.
- Presné riadenie hodnoty pH je nevyhnutné, pretože pri príliš vysokých hodnotách pH sa môžu iné kovy (napr. hliník) opäť stať rozpustnými.
Koncentrácia reagentov:
- Na viazanie všetkých iónov ťažkých kovov je potrebné dostatočné množstvo zrážadla. Predávkovanie však môže viesť k zvýšeným prevádzkovým nákladom a dodatočnej spotrebe chemikálií.
Teplota:
- Rýchlosť reakcie a rozpustnosť produktov zrážania závisia od teploty. Vyššie teploty zvyčajne podporujú rýchlosť reakcie.
Intenzita miešania a doba kontaktu:
- Dôkladné premiešanie zabezpečuje intenzívny kontakt medzi činidlami a iónmi ťažkých kovov.
- Doba kontaktu musí byť dostatočne dlhá, aby chemické reakcie mohli prebehnúť úplne.
Interferencie spôsobené inými iónmi:
- Anióny, ako je chlorid alebo síran, môžu zvýšiť rozpustnosť určitých zlúčenín ťažkých kovov a tým znížiť účinnosť zrážania.
- V takýchto prípadoch sú potrebné dodatočné precipitčné činidlá alebo kroky predbežnej úpravy.
Flokácia: stabilizácia a oddelenie produktov zrážania
Po zrážaní zostávajú vytvorené zrážacie produkty často rozptýlené vo vode vo forme jemných častíc. Flokácia slúži na zlučovanie týchto častíc do väčších agregátov (flokov), ktoré sa ľahšie usadzujú alebo oddeľujú.
Mechanizmus flokulácie
- koagulácia:
- Pridaním koagulantov, ako sú soli železa (III) alebo hliníka, sa znižujú elektrostatické odpudivé sily medzi časticami, čo uľahčuje ich aglomeráciu.
- flokácia:
- Flokulačné činidlá, ako sú polyméry (napr. polyakrylamidy), posilňujú tvorbu častíc tým, že spájajú vločky medzi sebou vytváraním mostíkov.
Limity zrážania a flokulácie
Komplexované ťažké kovy:
- Ťažké kovy, ktoré sa nachádzajú v stabilných organických alebo anorganických komplexoch, sa dajú len ťažko vysrážať. Je potrebné najskôr rozložiť komplexy (napr. oxidáciou alebo redukciou).
Zvyšné koncentrácie:
- Die chemische Fällung erreicht häufig nicht die extrem niedrigen Restkonzentrationen (< 0,01 mg/l) , die in manchen Industrien erforderlich sind. In solchen Fällen sind ergänzende Verfahren wie Adsorption oder Ionenaustausch erforderlich.
Produkcia bahna:
- Pri zrážaní vznikajú veľké množstvá zrážaného kalu, ktorý sa musí spracovávať a likvidovať ako nebezpečný odpad. Náklady na likvidáciu môžu byť značné.
Chróm(VI):
- Ťažké kovy, ako je chróm(VI), musia byť pred zrážaním redukované na menej toxickú formu chrómu(III), napríklad pridaním bisulfitu sodného.

Foto: Naše zariadenie CP ALMA CHEM MCW s precipitáciou a flokuláciou, odvodňovaním kalu a následným viacvrstvovým filtrom a iónovým výmenníkom (v prípade potreby)
2. Iónová výmena
Iónová výmena je fyzikálno-chemický proces, pri ktorom sa rozpustené ióny vo vode nahrádzajú iónmi v pevnej iónovej výmennej živici. Proces je založený na špecifickej väzbe katiónov alebo aniónov na aktívne skupiny v živicovom materiáli. Vďaka vysokej selektívnosti živíc je možné odstrániť ťažké kovy aj z veľmi zriedených roztokov.
Mechanizmus výmeny iónov
- výmena katiónov:
- Katióny ťažkých kovov, ako Cu²⁺, Zn²⁺ alebo Pb²⁺, sú nahradené iónmi H⁺ (vodíkové živice) alebo iónmi Na⁺ (sodíkové živice).
- Ťažký kov sa viaže na živicovú matricu a odstraňuje sa z vody.
- výmena aniónov:
- Komplexy ťažkých kovov s negatívnym nábojom, ako sú chromáty (CrO₄²⁻), sú nahradené iónmi OH⁻.
Druhy iónových výmenníkov
Silné katiónové výmenníky:
- Účinný pri odstraňovaní ťažkých kovov, ako je meď, nikel a zinok, z kyslých roztokov.
- Možné použitie pri hodnotách pH od 1 do 14.
Slabé katiónové výmenníky:
- Účinný pri stredných až vysokých hodnotách pH; ideálny pre mierne kyslé až neutrálne roztoky.
Silné aniónové výmenníky:
- Odstraňuje negatívne nabité komplexy, ako sú chrómáty alebo arzénáty.
- Použitie v alkalických roztokoch.
Selektívne živice:
- Vyvinuté pre špecifické ťažké kovy, ako je ortuť, kadmium alebo chróm.
Faktory ovplyvňujúce výmenu iónov
Koncentráciaiónov:
- Iónová výmena je obzvlášť účinná pri nízkych koncentráciách, pretože živice majú vysokú afinitu k iónom ťažkých kovov.
Hodnota pH:
- Der pH-Wert beeinflusst die Ladung der Schwermetalle und somit ihre Bindung an das Harz. Beispielsweise liegt Eisen bei pH < 3 als Fe³⁺ vor und kann leicht entfernt werden, während es bei höheren pH-Werten zu Hydroxid fällt.
Konkurencia:
- Prítomnosť iných katiónov, ako sú Ca²⁺ alebo Mg²⁺, môže znížiť účinnosť iónovej výmeny.
Kapacita živice:
- Maximálne zaťaženie živice je obmedzené jej špecifickou kapacitou (ekvivalentné ióny na objem).
Regenerácia:
- Po dosiahnutí kapacity sa živica regeneruje chemikáliami, ako je kyselina chlorovodíková (HCl) alebo hydroxid sodný (NaOH).
Výhody a obmedzenia iónovej výmeny
Výhody:
- Veľmi vysoká selektivita, aj pri nízkych koncentráciách ťažkých kovov.
- Regenerovateľný, čím sa znižujú prevádzkové náklady.
- Možno prispôsobiť konkrétnym kovom (napr. chrómu alebo medi).
Hranice:
- Obmedzená kapacita pri vysokých koncentráciách.
- Konkurencia iných iónov môže znížiť účinnosť.
- Regeneračné chemikálie vytvárajú dodatočné odpadové vody.

Foto: Naše zariadenie na výmenu iónov ALMA ION s predradeným filtrom s aktívnym uhlím ALMA FIL AK
3. Adsorpcia aktívnym uhlím
Adsorpcia pomocou filtrov s aktívnym uhlím je založená na fyzikálnej alebo chemickej adsorpcii iónov ťažkých kovov alebo komplexov ťažkých kovov na povrchu porézneho materiálu, ako je aktívne uhlie. Pri tom sa využíva veľký vnútorný povrch aktívneho uhlia na viazanie rozpustených látok z vody.
Mechanizmus adsorpcie
- Fyzikálna adsorpcia:
- Ťažké kovy sú zadržiavané na povrchu aktívneho uhlíka vďaka Van der Waalsovým silám alebo elektrostatickým interakciám.
- chemisorpcia:
- Ťažké kovy vytvárajú chemické väzby s funkčnými skupinami na povrchu aktívneho uhlia (napr. karboxylové alebo hydroxylové skupiny).
Druhy aktívneho uhlia
Aktívne uhlie v prášku (PAK):
- Jemný prášok, ktorý sa pridáva priamo do vody.
- Obzvlášť vhodné pre spracovanie dávok.
Granulované aktívne uhlie (GAK):
- Hrubozrnné aktívne uhlie, ktoré sa používa vo filtroch.
- Možné dlhodobé a nepretržité používanie.
Impregnované aktívne uhlie:
- Ošetrené chemickými činidlami (napr. sírou) na účinné odstránenie špecifických ťažkých kovov, ako je ortuť alebo arzén.
Faktory ovplyvňujúce adsorpciu
Koncentrácia ťažkých kovov:
- Vyššie koncentrácie vedú k lepšiemu využitiu adsorpčnej kapacity, ale aj k rýchlejšiemu nasýteniu.
Hodnota pH:
- Hodnota pH ovplyvňuje náboj iónov ťažkých kovov a povrchový náboj aktívneho uhlia.
- Príklad:
- Pri nízkej hodnote pH sú ťažké kovy ako Pb²⁺ kladne nabité a dobre sa viažu na záporné nabité aktívne uhlie.
Teplota:
- Adsorpčné procesy sú väčšinou exotermické, preto zvýšenie teploty môže znížiť ich účinnosť.
Pórovitá štruktúra:
- Veľkosť a rozloženie pórov v aktívnom uhlí ovplyvňujú väzbovú kapacitu.
Optimalizácia adsorpcie
- Predbežná úprava vody:
- Odstránenie suspendovaných látok a organických zlúčenín zvyšuje účinnosť.
- Použitie impregnovaného aktívneho uhlíka:
- Pre ťažké kovy, ako je arzén a ortuť, je výrazne účinnejšie špeciálne upravené aktívne uhlie.
- regenerácia:
- Sýtenie aktívneho uhlia možno zvrátiť tepelnými alebo chemickými postupmi, čím sa znížia prevádzkové náklady.
Výhody a obmedzenia adsorpcie aktívnym uhlím
Výhody:
- Vysoká účinnosť pri nízkych koncentráciách ťažkých kovov.
- Všestranné použitie, aj pre iné škodlivé látky, ako sú organické zlúčeniny.
- Môže byť špeciálne impregnovaný pre konkrétne ťažké kovy.
Hranice:
- Obmedzená kapacita adsorpčných materiálov.
- Regenerácia je energeticky a chemicky náročná.
- Menej vhodné pre vysoké koncentrácie ťažkých kovov.

Foto: Naše aktívne uhlíkové filtre ALMA FIL AK s predradenými viacvrstvovými filtrami ALMA FIL
Výzvy pri redukcii ťažkých kovov
Zvyšné koncentrácie:
- Ťažké kovy musia byť často redukované na veľmi nízke koncentrácie, čo je spojené s rastúcimi nákladmi.
- Zielwerte: z. B. Chrom < 0,05 mg/L, Nickel < 0,5 mg/L.
Hospodárenie s kalmi:
- Postupy ako chemická precipitácia produkujú veľké množstvá kalov, ktorých likvidácia je nákladná.
Komplexotvorné látky:
- Organické látky, ako napríklad EDTA alebo citráty, môžu stabilizovať ťažké kovy, čo sťažuje ich odstraňovanie.
Kombinácia technológií:
- V praxi sa často kombinuje viacero postupov, napr. zrážanie a adsorpcia, aby sa dosiahli optimálne výsledky.
Záver
Redukcia ťažkých kovov je podstatnou súčasťou priemyselného čistenia vody a odpadových vôd. V závislosti od špecifických požiadaviek a zloženia odpadových vôd sa používajú rôzne technológie. Pre vysoké koncentrácie kovov je vhodná precipitácia a flokulácia v CP zariadeniach a iónová výmena, zatiaľ čo pri jemnom čistení prevláda adsorpcia pomocou aktívnych uhlíkových filtrov. Starostlivé navrhnutie a monitorovanie procesu sú rozhodujúce pre dodržanie zákonných požiadaviek a trvalo udržateľnú ochranu životného prostredia.
Pre ďalšie informácie o našich produktoch nás môžete kedykoľvek kontaktovať!








